製品詳細
最終更新日:2024年5月31日
ユニツキシン®点滴静注17.5mg/5mLジヌツキシマブ(遺伝子組換え)
概要
-
製品名 ユニツキシン®点滴静注17.5mg/5mL 一般名 ジヌツキシマブ(遺伝子組換え) 先発製品名 ユニツキシン®点滴静注17.5mg/5mL 剤形 注射剤 規格 17.5mg5mL1瓶 成分・含量 1 バイアル中(5mL)ジヌツキシマブ(遺伝子組換え)17.5mg含有 薬効分類区分(保険薬辞典より) - 腫瘍用薬
- その他の腫瘍用薬
成分区分(保険薬辞典より) その他の抗悪性腫瘍用剤 規制区分 生物由来製品/劇薬/処方箋医薬品 製剤製造企業名 United Therapeutics Corporation(アメリカ)
薬価・厚生労働省コード・包装
-
薬価基準収載医薬品コード 4291457A1025 承認年月 2021.6.23 薬価基準収載年月 2021.8.12 発売開始年月 2021.9.22 先発後発区分 先発品 薬価(円) 1365888.00 包装単位 1バイアル(5mL)
最小包装単位 1バイアル(5mL)
JANコード 1バイアル(5mL) / 4987407374001
GS1コード 調剤包装単位 1バイアル(5mL) / 0104987407074000
販売包装単位 1バイアル(5mL) / 0114987407374008
統一商品コード 1バイアル(5mL) / 407374001
HOT番号 1バイアル(5mL) / 1991604010101
品質情報(最終更新日:2021/11/26)
-
生物学的同等性試験 ー 溶出試験 ー 安定性試験(加速試験) 安定性試験(苛酷試験等) 安定性試験(長期試験) 配合変化試験 ー 経管通過性試験 ー 粉砕(脱カプセル)後の安定性 ー
剤形(最終更新日:2021/09/22)
-
包装写真 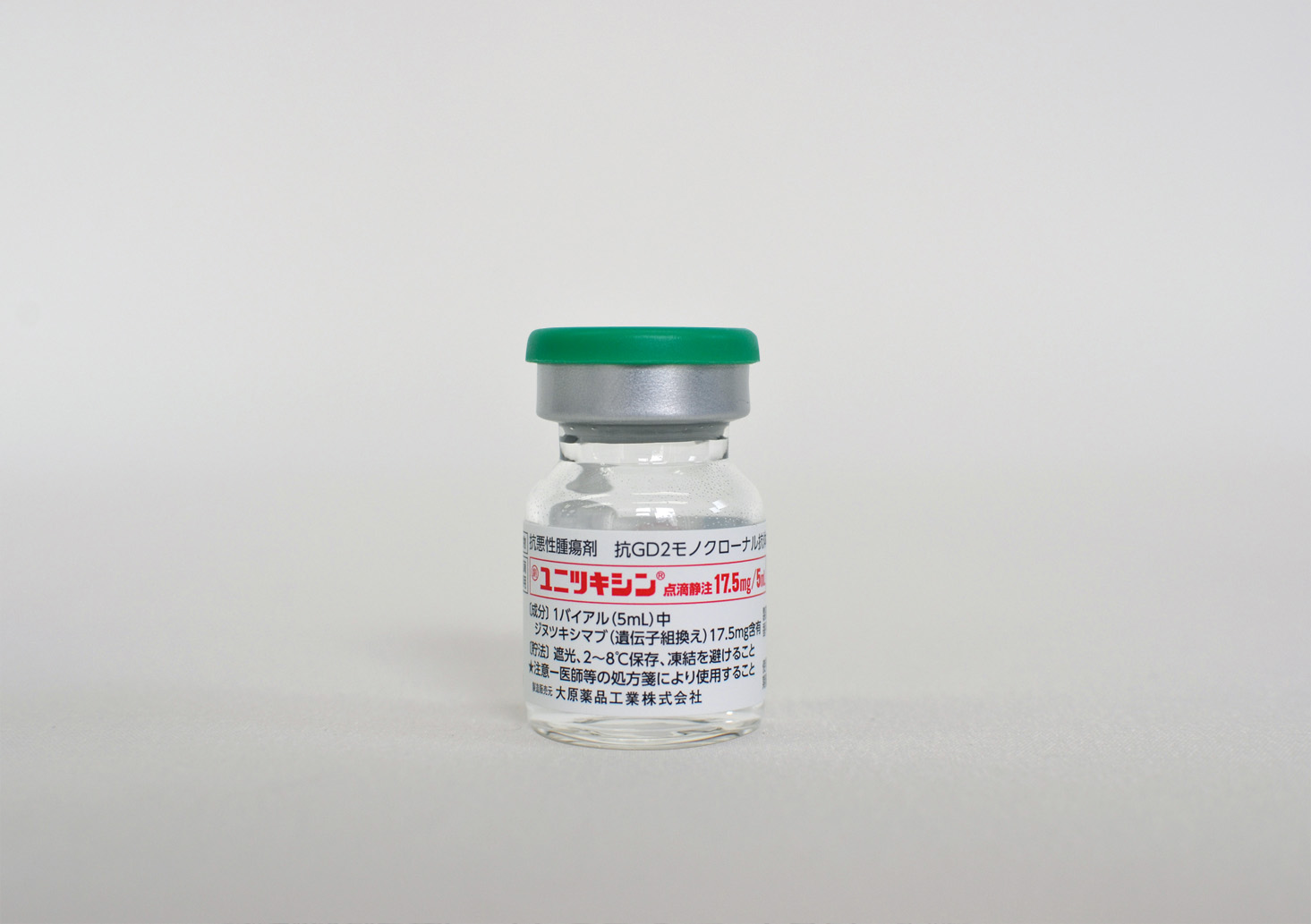
剤形/性状 水性注射剤 包装識別コード 該当しない 本体識別コード 該当しない
色調 無色澄明
保存
-
冷所保存 凍結を避け、2~8℃で保存 有効期間(年) 1.5